Så tar sig gifter in i cellerna – kapar näringsupptaget
Sjukdomsframkallande ämnen eller organismer, så kallade patogener, kapar cellernas upptagssystem för att ta sig in eller leverera toxiner (gifter). Upptagsvägarna används normalt av celler för att ta upp näring, receptorer och lipider. Det visar forskning vid Umeå universitet.
Forskningen visar även att cellernas upptagsvägar har en skyddande effekt vid skador på cellytan som orsakats av ett bakteriellt toxin.
– Behovet av läkemedel som på nya sätt angriper och behandlar infektioner är stort. Ett sätt kan vara att utveckla läkemedel som på olika sätt påverkar hur patogener interagerar med och påverkar cellens upptagssystem på cellytan, säger Lars Nygård Skalman, som är doktorand vid Institutionen för medicinsk kemi och biofysik och författare av avhandlingen.
Cellerna har flera olika endocytosvägar
Cellerna i kroppen kan ta upp näringsämnen men också reglera kompositionen av cellytan genom en transportprocess som kallas endocytos. Under denna process bildas inbuktningar i cellmembranet vilka sedan knoppas av som små blåsor, så kallade vesiklar.
En typisk human cell har flera olika typer av så kallade endocytosvägar. De olika vägarna används i olika situationer, regleras av olika proteiner samt varierar i både uppbyggnad samt i hur de aktiveras av olika typer av signaler. Forskning har kopplat endocytiska processer till flera allvarliga sjukdomar som muskeldystrofi, neurodegenerativa sjukdomar och cancer.
Dessa endocytiska processer är också viktiga vid infektioner eftersom virus, bakterier samt de infektionsframkallande toxiner och membranvesiklar som utsöndras av bakterier alla binder till olika molekyler på cellytan och därmed kapar specifika endocytosvägar för att ta sig in i våra celler.
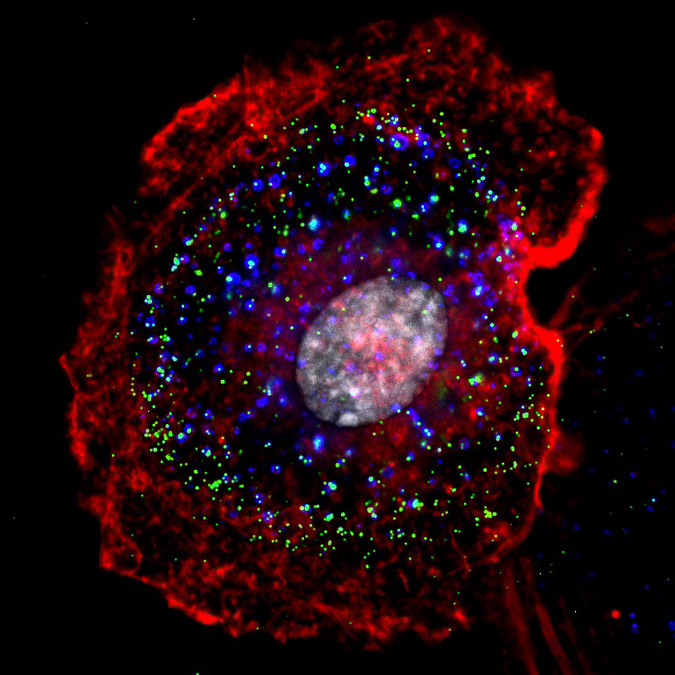
– Vår forskning visar att cellens endocytiska processer är av stor vikt i interaktionen med patogener och dess utsöndrande substanser. Genom att använda olika biokemiska och mikroskopibaserade metoder har vi kartlagt hur olika endocytosvägar är involverade i upptag av patogener men också vid reparation av cellmembranet, säger Lars Nygård Skalman.
Magsårsbakterien tar sig in i cellen via endocytosvägar
I sin avhandling visar Lars Nygård Skalman hur ögonviruset adenovirus 37 orsakar infektion i hornhinnan genom att interagera med specifika integriner, vilka är en typ av vidhäftningsproteiner på cellytan. Interaktionen är enligt forskaren troligtvis viktig för att viruset ska kunna ta sig in i cellen och replikera sig.
I en annan delstudie visar Lars Nygård Skalman att membranvesiklar från magsårsbakterien Helicobacter pylori, vilka finns i stor variation vad gäller både ytkomposition och storlek, kan använda olika endocytosvägar för att ta sig in i värdcellen.
I en tredje delstudie kartlagde Lars Nygård Skalman och forskarkollegorna hur olika endocytosvägar var inblandade i cellens förmåga att reparera skador i cellmembranet orsakade av ett porbildande toxin från bakterien Listeria monocytogenes. Om denna typ av skada inte repareras snabbt kan det leda till celldöd.
– Vi fann att flera endocytosvägar var viktiga för cellens förmåga att reparera skador som orsakats av listeriatoxinet. Men denna effekt beror förmodligen inte på att porerna tas bort från cellmembranet med hjälp av endocytos utan istället på de olika endocytosvägarnas förmåga att reglera kompositionen av cellmembranet, förklarar Lars Nygård Skalman.
Lars Nygård Skalman är ursprungligen från Hudiksvall. Han har en masterexamen i molekylärbiologi från Umeå universitet.
Avhandlingen: Pathogen entry mechanisms and endocytic responses to plasma membrane damage
Kontakt: Lars Nygård Skalman, Institutionen för medicinsk kemi och biofysik, Umeå universitet Telefon: 070-395 0930 E-post: lars.nygard.skalman@umu.se
Om disputationen: Fredagen den 19 maj försvarar Lars Nygård Skalman, Insititutionen för medicinsk kemi och biofysik sin avhandling med titeln: Hur patogener tar sig in i värdcellen samt rollen av endocytiska mekanismer vid skador på cellmembranet. Engelsk titel: Pathogen entry mechanisms and endocytic responses to plasma membrane damage. Opponent: Professor Kristian Riesbeck, Institutionen för translationell medicin, Lunds universitet, Malmö. Huvudhandledare: Universitetslektor Richard Lundmark. Disputationen äger rum kl. 13.00 i N320, Naturvetarhuset, Umeå universitet.